کریسپر: پایان تمام بیماریهای ژنتیکی
فهرست...
کریسپر (CRISPR) نام روشی درمانی است که میتواند بسیاری از بیماریهای ژنتیکی را در همان دوران کودکی از بین ببرد.
در ماه جولای سال ۲۰۱۹ میلادی، ویکتوریا گِری در اتاقی سبز رنگ در بیمارستانی واقع در مؤسسه پژوهشی سارا کانن در نشویل در حالی که سلولهای خونی ویرایش شدهی او کنار سرش در حال ذوب شدن بودند، از خواب بیدار شد. ویکتوریا گِری، زنی ۳۴ ساله از ایالت میسیسیپی است که ۴ فرزند دارد. وقتی که او ۳ ماهه بود، مادربزرگش متوجه فریادهای او شد و خیلی سریع او را از حمام بیرون آورد و به اورژانس برد. در آنجا پزشکان تشخیص دادند که ویکتوریا گِری به بیماری سلول داسی شکل (SCD) مبتلا است. سلول داسی شکل، نام یک اختلال ژنتیکی نادر است که به اندامهای اصلی بدن آسیب میرساند و باعث ایجاد دردهای طاقتفرسا در طول زندگی میشود. بیماری سلول داسی شکل از جهش ژن HBB بهوجود میآید. این جهش، دستورالعملها را تحریف میکند، بهطوریکه بدن بهجای ساخت یک جزء پروتئینی بهنام بتا-گلوبین برای انتقال اکسیژن، یک نسخه غیر طبیعی بهنام هموگلوبین S را تولید میکند.
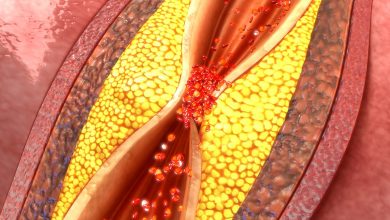
نتیجه: گلبولهای قرمز خون چسبناک و هلالی شکل میشوند. این خوشههای تیز در رگها تجمع میکنند و آنها را مسدود کرده یا پوشش آنها را از بین میبرند و میتوانند باعث وقوع حملات قلبی و مغزی حتی در کودکان شوند. در واقع پزشکان به مادر ویکتوریا گِری هشدار داده بودند که فرزند او نمیتواند بیش از ۶ سال زنده بماند. ویکتوریا گِری این بیماری را از والدین خود به ارث برده است. این بیماری از طریق ژنهای مغلوب سلول داسی شکل از پدر و مادر به فرزند منتقل میشود. اگر پدر و مادر در بدن خود این ژن مخرب را داشته باشند اما به بیماری سلول داسی شکل مبتلا نباشند، به احتمال ۲۵ درصد فرزند آنها به بیماری مبتلا میشود. اگر هم پدر و هم مادر بیماری سلول داسی شکل داشته باشند، تمام فرزندان آنها نیز به این بیماری مبتلا خواهند شد. این بیماری عمدتاً در افرادی دیده میشود که ریشه اجدادی آنها به آفریقا میرسد؛ زیرا پژوهشگران بر این باورند که در آفریقا، ژن سلول داسی شکل از بدن در برابر مالاریا بهشدت محافظت میکرده است.
حال، ویکتوریا گِری در بیمارستانی در نشویل روی تخت نشسته است و آماده میشود تا سرنوشت شوم DNA خود را برای همیشه تغییر دهد.
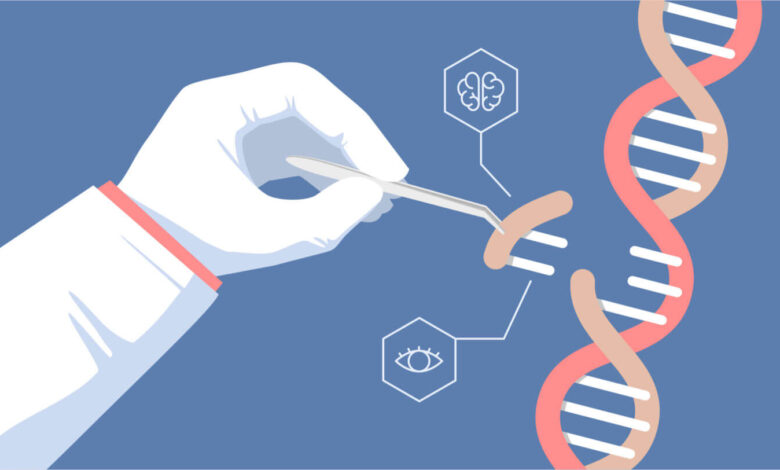
اصلاح ژن با قیچیهای ژنتیکی
چند هفته قبل از تزریق، حیدر فرانگول، پزشک ویکتوریا گِری و مدیر واحد پزشکی هماتولوژی کودکان در مؤسسه پژوهشی سارا کانن، میلیاردها سلول بنیادی ویکتوریا گِری را استخراج کرده و آنها را به آزمایشگاهی در اروپا فرستاده بود. در آنجا، دانشمندان با استفاده از پالسهای الکتریکی، بهطور موقت منافذی را در غشای سلولهای وی ایجاد کردند. آنها سپس «قیچیهای مولکولی» را از طریق منافذ ایجاد شده وارد غشای سلول کردند تا کدهای ژنتیکی مخرب را اصلاح کنند. پس از انجام این کار، سلولهای مهندسی شده منجمد شدند و به نشویل فرستاده شدند. سلولهای خونی اکنون در نشویل و در کنار ویکتوریا گِری در حال ذوب شدن هستند. دکتر فرانگول به کمک یک سرنگ، سلولها را به خط مرکزی منتهی به سینهی ویکتوریا گِری تزریق کرد. هنگام تزریق، نبض ویکتوریا گِری تندتر شد و این در حالی بود که سلولهای ویرایش شده تولید یک فرم هموگلوبین سالم را آغاز میکردند. دکتر فرانگول قول داده بود که این روش میتواند ویکتوریا گِری را از یک عمر درد و ناراحتی قلبی نجات دهد؛ دردی که او را مجبور میکرد در اوایل ۳۰ سالگی هر ماه به بیمارستان مراجعه کند.

تکنیک پیوندی بهکار رفته برای غلبه بر کدهای ژنومی مسئول بیماری سلول داسی شکل CRISPR-Cas9 نام دارد. این یک روش سادهتر، ارزانتر و دقیقتر از فنآوریهای ویرایش ژنتیکی است که در دههی ۹۰ میلادی ظاهر شدند اما هیچگاه نتوانستند به موفقیت چشمگیری دست یابند. این روش میتواند به ما در ریشهکن کردن بیماریهای ارثی همچون سندروم داون، نابینایی، دیسلکسیا و فیبروز کیستیک کمک شایانی کند.
اریک آلسون، استاد و زیستشناس مولکولی از دانشگاه تگزاس میگوید:
کریسپر به شما این امکان را میدهد تا برای هر ارگانیسمی که میخواهید، نقشه حیات را تغییر دهید.
در حالت فرضی، میتوان از روش کریسپر (حتی در جنین) در مناطق خاصی از کروموزوم برای تغییر و شخصیسازی صفات جسمی، ذهنی و مولکولی فرد استفاده کرد. بهعنوان مثال، ممکن است که در آینده بتوان به کمک این روش، رنگ مو یا رنگ چشم کودک را تعیین کرد. حتی کریسپر میتواند امکان دستکاری سطح هوش و یا بیماری اوتیسم را فراهم کند؛ زیرا ما میدانیم که این دو، تا حد زیادی به ژنتیک و عوامل محیطی بستگی دارند.
اما برای ویکتوریا گِری، کریسپر یک روزنهی امید است. تلاش او برای انجام پیوند مغز استخوان تا کنون ناموفق بوده است. پیوند مغز استخوان تنها درمان فعلی برای سلول داسی شکل بهشمار میرود که بسیار پرخطر است. زمانی که او امید خود را از دست داده بود، دکتر فرانگول به او پیشنهادی داد؛ وی گفت که اگر ویکتوریا گِری موافق باشد، میتواند به یکی از اولین انسانها در سراسر جهان تبدیل شود که این روش درمانی را بهصورت تجربی امتحان میکند. دکتر فرانگول میگوید که ما حتی از کارکرد این روش مطمئن نبودیم اما ویکتوریا گِری اصرار داشت که داوطلب شود.
کریسپر چگونه کار میکند؟
حدود یک دهه پیش، دکتر جنیفر داودنا مشغول مطالعهی باکتریها در پتری دیش بود که به چگونگی مبارزهی باکتریها با ویروسها پی برد و آن را رمزگشایی کرد. بهطور دقیق، این متخصص بیوشیمی دریافت که این باکتریها و سایر میکروارگانیسمها با بهخاطر سپردن توالی DNA مهاجمان پیشین، از خود در برابر عفونتها دفاع میکنند؛ بنابراین هنگام بازگشت ویروسها، سیستم ایمنی بدن دقیقاً برای غلبه بر آنها آماده میشود.
کریسپر یا به اختصار «تناوبهای کوتاه پالیندروم فاصلهدار منظم خوشهای»، بخشی از سیستم ایمنی باکتریایی است. پالیندروم در اینجا یعنی توالی DNA که بتوان آن را قرینهخوانی کرد؛ یعنی هم از عقب و هم از جلو به شکلی یکسان خوانده شود.
باکتریها برای بهخاطر سپردن آن کد ژنتیکی خاص، بخشهایی از کدهای ژنتیکی عامل مهاجم را که «جداساز» نامیده میشوند، میدزدند. سپس آنها را درون DNA، جداسازها و تناوبهای خود قرار داده و ساختن کپیها یا مولکولهایی تک رشتهای به نام RNA را آغاز میکنند. این رشتههای کوتاه RNA کریسپر هنگام شناسایی یک ویروس، بهعنوان یک راهنما جهت شناسایی توالی ویروسی عمل میکنند. سپس قطعه دیگری از سیستم کریسپر که یک آنزیم بهنام Cas9 است، ویروس را برش داده و از بین میبرد تا قادر به تکثیر نباشد.
در سال ۲۰۱۲، دکتر جنیفر داودنا، استاد دانشگاه کالیفرنیا مقالهای پیشگامانه در توصیف این مانور منتشر کرد. این مقالهی مهم، کریسپر را بهطور رسمی به یک فرهنگ لغت پزشکی گسترده تبدیل کرد. در سال ۱۹۸۷، پژوهشگران ژاپنی یک توالی DNA تکرارشوندهی غیرمعمول را در باکتری «اشریشیا کلی» شناسایی کرده بودند؛ بنابراین دانشمندان با توجه به چنین مشاهداتی، یک تصور و پیشزمینه نسبی از کریسپر داشتند. اما این دکتر جنیفر داودنا بود که موفق به کدگشایی کریسپر شد و توانست کریسپر را به یک ابزار کنترل زیستی تبدیل کند. او توانست کریسپر را به ابزاری تبدیل کند که میتواند توالیهای ژنوم را به سادگی رفع یک غلط املایی در جمله، اصلاح کند.
پروفسور اریک آسلون، زیستشناس مولکولی از دانشگاه تگزاس که درمانهای مبتنی بر کریسپر را برای دیستروفی ماهیچهای توسعه داده، بر این باور است که به کمک کریسپر میتوان نقشهی حیات را برای هر ارگانیسمی تغییر داد و این قطعاً تأثیری طولانی مدت بر زندگی خواهد داشت و نمیتوان آن را نادیده گرفت. در سال ۲۰۲۰ دکتر جنیفر داودنا به همراه پروفسور امانوئل شارپنتیه که اکنون مدیر واحد علوم پاتوژن در مؤسسهی ماکس پلانک در برلین است، موفق شدند بهطور مشترک برندهی جایزهی نوبل شیمی برای کار علمی تحول آفرین در «بازنویسی کد زندگی» شوند.
قسمت خطرناک کریسپر
تا به امروز، زیستشناسان از کریسپر در موارد زیر استفاده کردهاند:
- ایجاد بزهای چاق با موهای بلند جهت تولید گوشت و پشم بیشتر
- ایجاد باکتریهای نگهبان جهت مقاوم کردن پنیر و ماست در برابر عفونتهای ویروسی
- حذف ژن کافئین در گیاهان قهوه
- تولید گونهای از خوکهای کوچک که حیوان خانگی هستند
در ماه نوامبر سال ۲۰۱۸، یک دانشمند چینی بهنام جیانکوی هه، ویدیویی را در یوتیوب بارگزاری کرد و در آن از متولد شدن نخستین کودک اصلاح شده با کریسپر خبر داد. این تأییدی بر انجام آزمایش انسانی کریسپر بود و بسیار جنجال برانگیز شد. وی ادعا کرد که جنین دختران دوقلو را با استفاده از روش کریسپر دستکاری کرده است تا در برابر HIV مقاوم باشند. پس از اصلاح ژنتیکی، رویان مجدداً در رحم مادر کاشته شد. بیماری HIV در چین ننگی بزرگ محسوب میشود. این خبر بهسرعت در سراسر جهان پخش شد و واکنش تند دانشمندان و روحانیون مذهبی را به دنبال داشت. دانشمندان خواستار توقف جهانی استفاده از کریسپر روی جنین، تخمک یا اسپرم برای ایجاد نوزادان اصلاح شده ژنتیکی شدند. تا به امروز اگرچه بسیاری از کشورها این عمل را منع کردهاند؛ اما هنوز مجازاتی برای انجام آن در نظر گرفته نشده است. با وجود این، دولت چین جیانکوی هه را به ۳ سال زندان محکوم کرد. طولی نکشید که دانشمندی دیگر، اینبار در روسیه به خبرنگاران گفت که میخواهد از یک طرح ویرایش جنین مشابه استفاده کند تا به زوجهایی که ژن ناشنوایی مادرزادی دارند، این امکان را بدهد که فرزندی با شنوایی طبیعی داشته باشند.
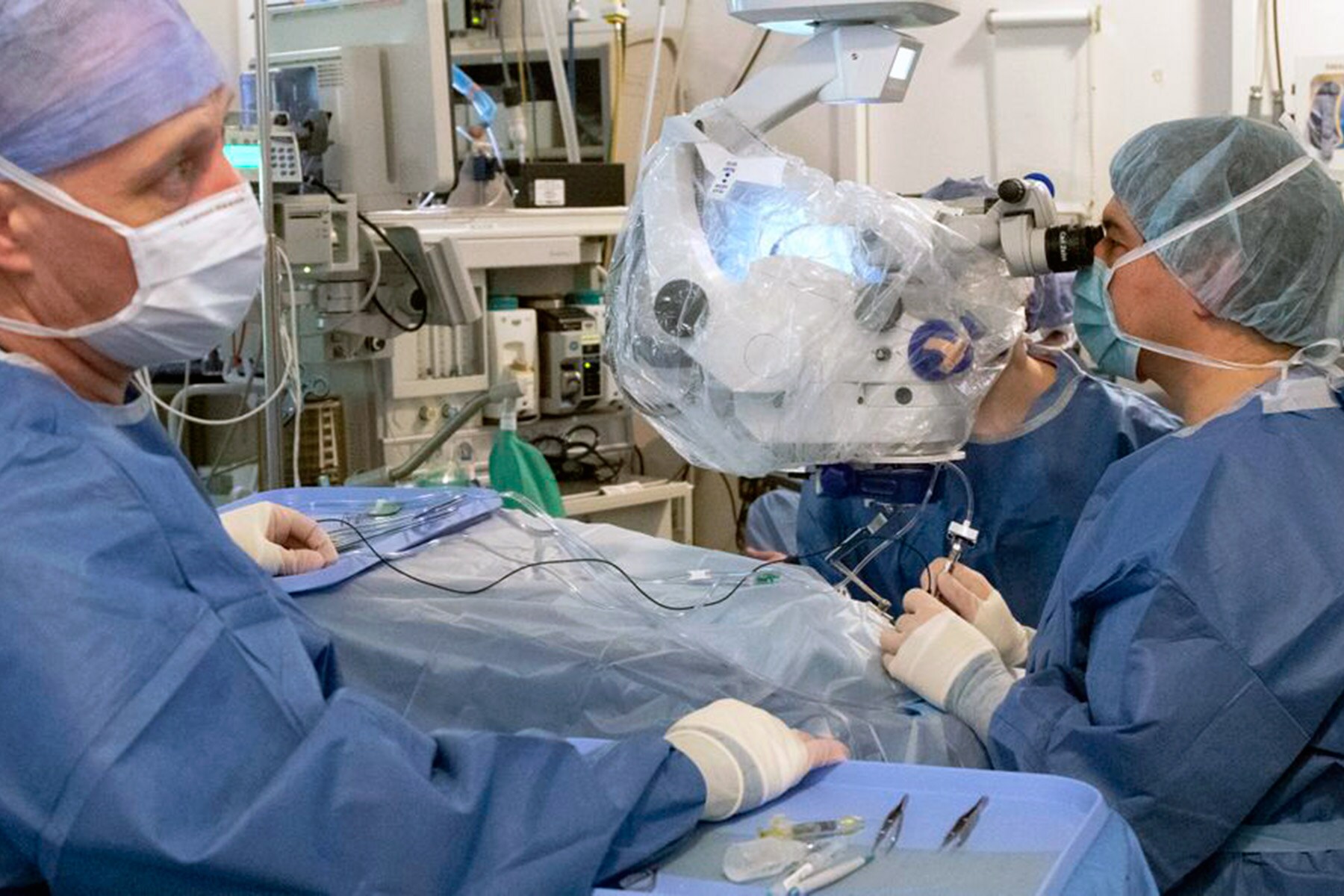
کریسپر پتانسیل گستردهای دارد؛ اما مسئلهی اخلاقی، معضلی است که اکنون جامعهی علمی با آن مواجه است. مرز میان از بین بردن رنج انسان (غیرقابل بازگشت) و دستکاری ترکیب ژنتیکی نسلهای آینده باید کجا باشد؟
روشی که جیانکوی هه برای دوقلوهای چینی بهکار برد «ویرایش خط جوانهزنی» نام دارد. این روش روی جنینها انجام میشود و تغییرات DNA حاصل از آن دائمی و وراثتی میشوند. جیانکوی هه بهنوعی پیشگام آزمایشهای انسانی کریسپر است. در سال ۲۰۲۰ دانشمندان در اورگان آمریکا قطرهای که ابزار ژنتیکی کریسپر در آن جاسازی شده بود را به شبکیه چشم یک بزرگسال که با نوعی نادر از نابینایی ارثی متولد شده بود ریختند. قطره برای ترمیم ژنی بهنام CEP290 برای بازگرداندن بینایی طراحی شده است. کودکان و بزرگسالان مبتلا به نابینایی در سراسر جهان در انتظار نتایج اولیهی این آزمایش هستند که قرار است اواخر سال جاری منتشر شوند. این نخستینباری بود که پزشکان از کریسپر در داخل بدن انسان زنده یا ویرایش ژن «درونجانداری» استفاده کردند. بیمار هنوز ژن نابینایی را در بدن خود دارد؛ بنابراین ممکن است فرزند آن نیز نابینا به دنیا بیاید.
بهطور قطع، کریسپر وسیلهای برای دستیابی به یک هدف منطقی است: اصلاح، درمان یا معکوس کردن جهشهای ژنتیکی که باعث بیماری یا زندگی کوتاه مدت میشوند. ژن درمانیهای قدیمی بسیاری از بیماریها را درمان میکردند؛ اما کریسپر وسعت بسیار بیشتری دارد و میتواند بیماریهای ارثی را از استخر ژن بهطور کامل پاکسازی کند. این آیندهی روشن، ممکن است با عواقب ناخواسته یا «اثرات خارج از هدف» همراه باشد.
پروفسور اینسو هیون، مدیر واحد پژوهش اخلاقی در مرکز اخلاقزیستی دانشکده پزشکی هاروارد پرسشی بسیار مهم را مطرح میکند که باعث میشود در مورد روش کریسپر اندکی تأمل کنیم:
یکی از پرسشهای اخلاقی که در جریان پژوهش در هر زمینهای مطرح میشود این است که چه کسی حاضر است خطرات و مزایای یک فناوری جدید را تحمل کند؟ در مورد ویرایش ژنتیکی و حذف ژنهای مشکلدار، قطعاً این زن و شوهر هستند که از مزیتهای آن بهرهمند میشوند؛ اما به احتمال زیاد خطرات آن متوجه نوزاد متولد نشده و فرزندان او خواهد شد. از نظر فلسفی: آیا ما حاضر هستیم که مسیری که پا در آن نهادهایم را تا آخر برویم؟
بهطور خلاصه، بله ما همین الآن هم حاضر به انجام این کار هستیم!
دانشمندان با آزمایش روی موشها نشان دادهاند که کریسپر میتواند علائم سندروم X شکننده (یکی از دلایل ژنتیکی اوتیسم که میتواند منجر به حساسیت شدید به نور و صدا و رفتارهای وسواسی و تکراری شود) را بهطور کامل مهار کند. همچنین کریسپر توانسته بهطور کامل سگهای مبتلا به دیستروفی ماهیچهای دوشن (یک بیماری نادر تحلیل عضله که بیشتر پسران را درگیر میکند) را درمان کند. بهزودی درمانهای مشابه نیز روی انسانها انجام خواهد گرفت. هیچ کسی به اندازه والدین فرزندانی که بیماریهای مادرزادی ویرانگر دارند، منتظر فرارسیدن این آیندهی روشن نیست.
امیدها برای درمان در آینده
هاوکن میلر، کودکی سالم و طبیعی بود که به هنگام تولد ۴.۹ کیلوگرم وزن داشت. وقتی که او ۴ ساله بود، مادرش او را دید که هنگام تمرین فوتبال گریه میکند. هاوکن میلر از شدت درد به خود میپیچید و وضعیتی غیرعادی داشت. مادرش پس از اطمینان از بروز مشکلی جدی، او را نزد متخصص اطفال برد. نزدیک به یک سال طول کشید تا اینکه پزشکان بالاخره توانستند تشخیص دهند هاوکن میلر کوچک، به دیستروفی ماهیچهای دوشن مبتلا است. این بیماری دژنراتیو (فرسایشی تخریبی) از جهش در بزرگترین ژن در بدن انسان، یعنی ژن دیستروفین ناشی میشود. پسرانی که به دیستروفی ماهیچهای دوشن مبتلا هستند، به هنگام تولد بسیار سالم بهنظر میرسند و مشکلی ندارند؛ اما از آنجایی که بدن آنها فاقد یک پروتئین حیاتی (پروتئینی که نقش کمک فنر عضلات را بر عهده دارد) است، تا پیش از دورهی پیش دبستانی تقریباً تمام بافت عضلانی آنها از بین میرود. این بیماری پیشرونده است و متوقف نمیشود. در دوران راهنمایی بسیاری از پسرانی که به آن مبتلا هستند دیگر نمیتوانند راه بروند. در بزرگسالی، آنها برای نفس کشیدن به ونتیلاتور احتیاج پیدا میکنند.
هاوکن میلر اکنون ۲۴ ساله است و بهطور مستقل در شهر لس آنجلس زندگی میکند و به کار روزنامهنگاری در زمینهی سلامت مشغول است. او به کمک ویلچر جابهجا میشود، با دستگاه تنفس میخوابد و هر روز دو داروی مختلف برای ضعف قلب خود مصرف میکند. میانگین طول عمر برای مرد مبتلا به دیستروفی ماهیچهای دوشن فقط ۳۰ سال است. مادر هاوکن میلر میگوید سختترین قسمت ماجرا برای یک مادر این است که میبیند فرزندش روز به روز ضعیفتر میشود و بدنش تحلیل میرود.

مادر هاوکن میلر، اندکی پس از تشخیص بیماری در فرزند خود بنیادی بهنام «CureDuchenne» تأسیس کرد. این بنیاد به کمک پروفسور اریک آسلون، زیستشناس مولکولی از دانشگاه تگزاس توانسته تا به امروز ۲ میلیون دلار سرمایه جهت کشف درمان مبتنی بر کریسپر برای دیستروفی ماهیچهای دوشن جمعآوری کند.
در جدیدترین آزمایش، گروه پروفسور آسلون ویروسی بیخطر حاوی ژنهای ویرایش شدهی کریسپر را به بدن ۶ سگ که ژن دوشن داشتند تزریق کرد. در داخل بدن، آنزیمی برای منطقه ژن معروف به اگزون ۵۱ شروع به خطزنی و برش کرد. در عرض چند هفته، سگها شروع به تولید پروتئین از دست رفته کردند. پروفسور آسلون بر این باور است که این لحظهای بزرگ و بسیار مهم است؛ زیرا با توجه به نتایج امیدوار کنندهای که حاصل شده، میتوان امید داشت کودکانی که به این بیماری مبتلا هستند تا چند سال آینده بتوانند به کمک کریسپر درمان شوند. متأسفانه او میگوید که کریسپر نمیتواند ماهیچهای که از بین رفته است را مجدداً بازیابی کند. متأسفانه مادر هاوکن میلر نیز میداند که دیگر برای درمان پسرش دیر شده است و اگر هاوکن کودک بود میشد به درمان آن امیدوار بود.
یک زندگی که بهطور کامل ترمیم شد
به ماجرای ویکتوریا گِری باز میگردیم. اکنون ۲ سال از زمانی که از روش کریسپر برای بیماری سلول داسی شکل او استفاده شد، میگذرد.
سلولهای بنیادی ویرایش شدهی ویکتوریا گِری در مغز استخوان و خون او ریشه دوانده است و خیلی زود، هموگلوبین داسی شکل جای خود را بهطور کامل به هموگلوبین سالم داد و علائم بیماری کاملاً ناپدید شد.
حیدر فرانگول، پزشک ویکتوریا گِری و مدیر واحد پزشکی هماتولوژی کودکان در مؤسسه پژوهشی سارا کانن میگوید:
اکنون ما بهعنوان جامعهی پزشکی با یک پرسش اساسی مواجه هستیم: دقیقاً چه زمانی باید برای درمان با کریسپر مداخله کرد؟ قبل از تولد یا بعد از آن؟
آیا روزی فرا میرسد که بتوان از کریسپر برای ویرایش ژن سلول داسی شکل در جنین استفاده کرد تا هیچ کودکی با این بیماری متولد نشود؟ دکتر فرانگول اطمینان دارد که انجام چنین کاری ممکن است.
هنوز مسائل اخلاقی قضیه پابرجا هستند؛ اما آنچه که واضح است کارمد بودن کریسپر و مزایای بیشمار آن است. اکنون هیچ کسی مانند ویکتوریا گِری از این درمان رضایت ندارد. او که تمام زندگی خود را در راه بیمارستانها بوده و درد بسیار زیادی را تحمل کرده است، حال به کمک کریسپر درمان شده و میتواند از کارهایی لذت ببرد که تا پیش از آن نمیتوانسته لذتی از آنها ببرد. او اکنون میتواند شاهد تشویق کردن دختر خود و مسابقه فوتبال پسرش باشد. او اکنون از زندگی لذت میبرد.